31 Jul 2025
Silberrückgewinnung

Silber und Original-Fotopapier
Silber ist ein wesentlicher Bestandteil für die Qualität von Drucken auf Original-Fotopapier. Silber ist Teil der fotografischen Schicht, die in Gelatine eingebettet ist. Wenn das Silber (Silberhalogenidkristalle) im Fotopapier belichtet wird, entsteht durch ein RGB-Belichtungssystem ein latentes Bild. Das Fotopapier durchläuft dann einen RA4-Entwicklungsprozess unter Verwendung eines Entwicklers und eines Bleich-Fixierers, um das Bild auf dem Papier zu erzeugen. Während dieses Prozesses bilden sich in drei verschiedenen Schichten Cyan-, Magenta- und Gelbfarbstoffe.
Wie gewinnen wir das Silber aus dem Papier zurück?
Während des RA4-Entwicklungsprozesses werden etwa 99 % des im Foto vorhandenen Silbers entfernt. Aber wohin geht es?
Der größte Teil dieses Silbers, etwa 96 %, gelangt in die Bleich-Fixier-Lösung, wo es sich mit Thiosulfat-Ionen zu Komplexen verbindet. Dieses Silber kann von den meisten großen Fotolabors durch elektrolytische Entsilberung intern zurückgewonnen werden. Einige Fotolabors entscheiden sich möglicherweise dafür, die chemischen Abfälle zu sammeln und von einem Entsorgungsunternehmen entsorgen zu lassen.
Die restlichen 3 % des Silbers aus dem RA4-Entwicklungsprozess gelangen in das Waschwasser. Um zu verhindern, dass dieses Silber in den Abfluss gelangt, setzen einige Fotolabore ein Ionenaustausch-Entsilberungssystem ein. Dieses System nutzt Ionenaustauschharze, die selektiv Silberionen aus dem Waschwasser auffangen, sodass diese zurückgewonnen und wiederverwendet werden können. Dieser interne Entsilberungsprozess stellt sicher, dass das Silber ordnungsgemäß entsorgt wird, anstatt von einer regionalen Kläranlage behandelt zu werden.
Soweit der einfachste Teil der Silberrückgewinnung. Kommen wir nun zum technischen Teil:
Elektrolytische Silberrückgewinnung aus einem Bleich-Fixiermittel auf Thiosulfatbasis
Silber ist in der Bleich-Fixier-Lösung in Form von Komplexen mit Thiosulfat-Ionen vorhanden, die sich im Gleichgewicht dissoziieren können, um Silberionen und Thiosulfat-Ionen freizusetzen.
An der Kathode, einer negativ geladenen Elektrode, werden die Silberionen durch Aufnahme von Elektronen reduziert und bilden festes Silber. Die Reaktion lässt sich wie folgt darstellen: Ag + + e –> Ag.
An der Anode, einer positiv geladenen Elektrode, können mehrere Reaktionen stattfinden.
Wichtige Reaktionen an der Anode sind die Oxidation von Thiosulfat und Sulfit. Zusätzlich findet an der Kathode die Reduktion von Eisen statt.
Diese Reaktionen tragen gemeinsam zur Verringerung der Konzentration von Thiosulfat, Sulfit und pH-Wert in der Bleich-Fixier-Lösung bei. Die Wirksamkeit der Bleich-Fixier-Lösung kann durch Belüftung wiederhergestellt werden, wodurch inaktive Fe2+-Ionen in aktive Fe3+-Ionen umgewandelt werden.
Um eine effektive Entsilberung zu gewährleisten, ist eine ausreichende Bewegung erforderlich, um die Bildung von Silbersulfid an der Kathode zu verhindern.
Gelatine ist nur bis zu etwa 2 % des Silbergewichts wünschenswert, da ein Überschuss ebenfalls zu einer Sulfidierung führen kann.
Es ist wichtig zu beachten, dass die Entsilberung in Bleich-Fixier-Lösungen aufgrund der Beteiligung von Eisen-III- und Eisen-II-Reaktionen schwieriger ist als die Fixiermittelrückgewinnung. Um der Reoxidation von Eisen entgegenzuwirken, wird in der Regel ein Hochstromsystem eingesetzt.
Ein weniger häufig verwendetes alternatives kontinuierliches Entsilberungssystem ist das PSR (Ilford) Electrogen. Dieses System nutzt die kontrollierte Reduktion von Eisen III zu Eisen II unter Verwendung von Natriumdithionit. Um eine präzise Dosierung zu gewährleisten, werden eine Sonde und eine Dosiereinheit verwendet, um die Zugabe von überschüssigem Reagenz zu verhindern. Die Zugabe von zu großen Mengen Natriumdithionit kann zur Ausfällung von Silber führen. Umgekehrt kann es bei einem Mangel an Natriumdithionit zu einer fehlerhaften oder gar keiner Beschichtung kommen, insbesondere da die Beschichtungseinheit für eine niedrige Stromdichte ausgelegt ist.
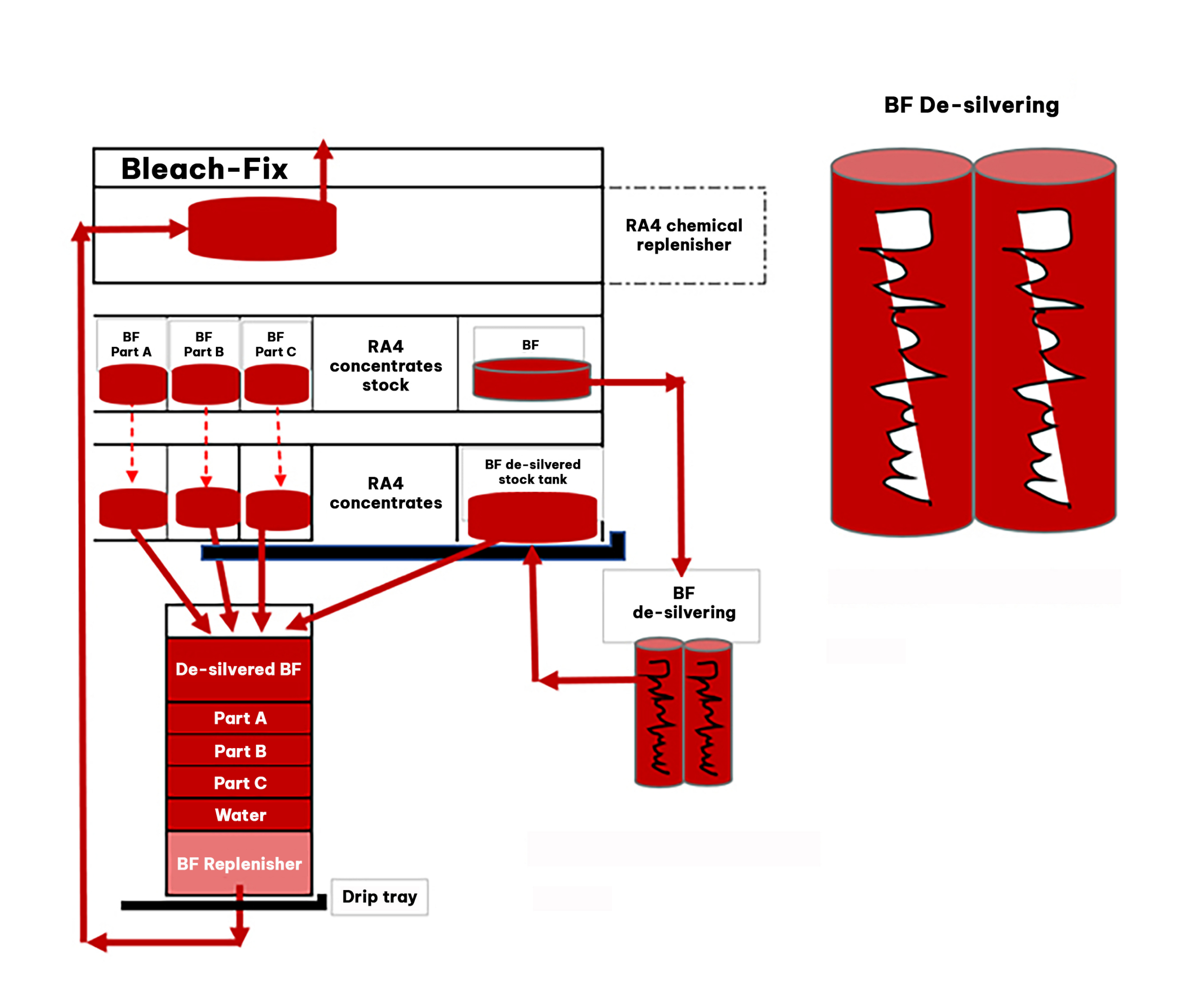
Aufbau zur elektrolytischen Silberrückgewinnung :
Silberrückgewinnungsraten und -effizienz
Durch Anwendung des Faradayschen Gesetzes ermöglichen diese Berechnungen eine Abschätzung der potenziellen Silberrückgewinnung und -effizienz bei der elektrolytischen Entsilberung.
Masse der Substanz = (Strom × Zeit × Äquivalentmasse) / (Faradaysche Konstante)
Beispielrechnung Potenzielle Rückgewinnung: 100 A *3600 s *107,87 / 96485 = 100 A*4,02 = 402 g Ag pro Amperestunde
- Potenzielle Rückgewinnung (Gramm Ag pro Amperestunde) = Strom x 4,02
- Theoretische Rückgewinnung %= (Potenzielle Rückgewinnung / Ag in) x 100
- Tatsächliche Rückgewinnung % = (Ag_out / Ag_in) x 100
- Effizienz % = (Tatsächliche Rückgewinnung / Theoretische Rückgewinnung) x 100