31 Jul 2025
Recuperación de plata

Plata y papel fotográfico original
La plata es un componente esencial para la calidad de las impresiones en papel fotográfico original. La plata forma parte de la capa fotográfica, incrustada en gelatina. Cuando la plata (cristales de haluro de plata) del papel fotográfico se expone, se crea una imagen latente mediante un sistema de exposición RGB. A continuación, el papel fotográfico se somete a un proceso de revelado RA4 utilizando un revelador y un fijador-blanqueador para crear la imagen en el papel. Durante este proceso, se forman tintes cian, magenta y amarillo en tres capas diferentes.
¿Cómo recuperamos la plata del papel?
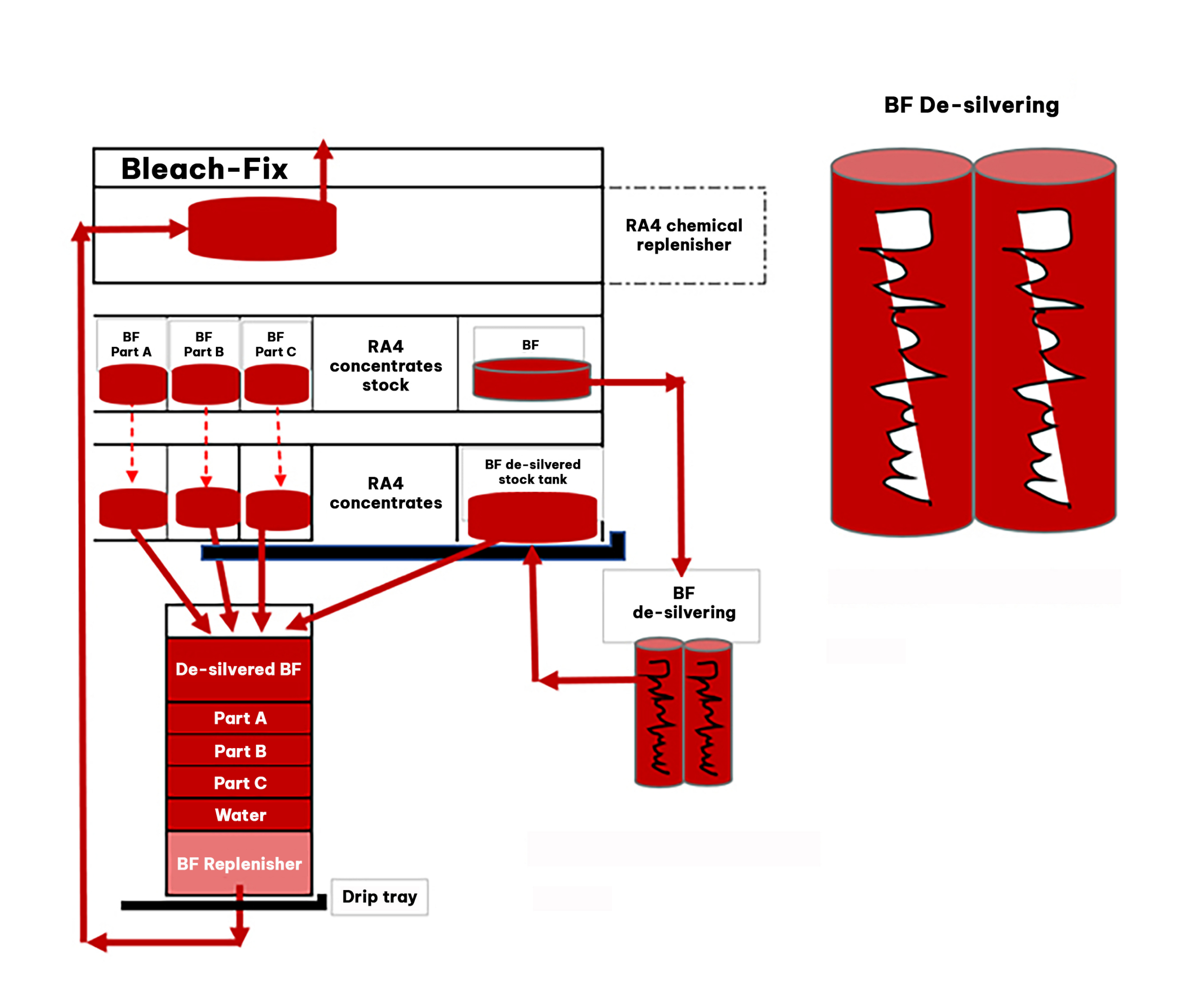
Durante el proceso de revelado RA4, se elimina aproximadamente el 99 % de la plata presente en la fotografía. Pero, ¿adónde va a parar?
La mayor parte de esta plata, alrededor del 96 %, termina en la solución blanqueadora-fijadora, donde se combina con iones de tiosulfato para formar complejos. La mayoría de los grandes laboratorios fotográficos pueden recuperar esta plata internamente mediante un proceso de desargentación electrolítica. Algunos laboratorios fotográficos pueden optar por recoger los residuos químicos para que los gestione una empresa de gestión de residuos.
El 3 % restante de la plata del proceso de revelado RA4 acaba en el agua de lavado. Para evitar que esta plata se pierda por el desagüe, algunos laboratorios fotográficos emplean un sistema de desarguración por intercambio iónico. Este sistema utiliza resinas de intercambio iónico que capturan selectivamente los iones de plata del agua de lavado, lo que permite su recuperación y reutilización. Este proceso interno de desarguración garantiza que la plata se gestione adecuadamente en lugar de ser tratada por una planta regional de tratamiento de aguas.
Hasta ahora, esta es la parte más fácil de la recuperación de plata.
Ahora profundicemos en la parte técnica:
Recuperación electrolítica de plata a partir de un fijador-blanqueador a base de tiosulfato
La plata está presente en la solución fijadora-blanqueadora en forma de complejos con iones de tiosulfato, que pueden disociarse en equilibrio para liberar iones de plata e iones de tiosulfato.
En el cátodo, que es un electrodo con carga negativa, los iones de plata se reducen al ganar electrones para formar plata sólida. La reacción se puede representar como: Ag + + e –> Ag.
En el ánodo, que es un electrodo con carga positiva, pueden producirse varias reacciones.
Las reacciones importantes en el ánodo son la oxidación del tiosulfato y el sulfito. Además, en el cátodo se produce la reducción del hierro.
Estas reacciones contribuyen colectivamente a la reducción de la concentración de tiosulfato, sulfito y pH en la solución blanqueadora-fijadora. La eficacia de la solución blanqueadora-fijadora puede restaurarse mediante aireación, que convierte los iones Fe2+ inactivos en iones Fe3+ activos.
Para garantizar una desargentación eficaz, es necesario agitar suficientemente para evitar la formación de sulfuro de plata en el cátodo.
La gelatina solo es deseable hasta aproximadamente el 2 % del peso de la plata, ya que un exceso también puede provocar sulfuración.
Es importante señalar que la desargentación en soluciones de blanqueador-fijador es más difícil que la recuperación del fijador, debido a la participación de reacciones de hierro III y hierro II. Para contrarrestar la reoxidación del hierro, se suele emplear un sistema de alta corriente.
Un sistema alternativo de desargentación continua menos utilizado es el PSR (Ilford) Electrogen. Este sistema emplea la reducción controlada del hierro III a hierro II utilizando ditionito de sodio. Para garantizar una dosificación precisa, se utiliza una sonda y una unidad de dosificación para evitar la adición de un exceso de reactivo. La adición de cantidades excesivas de ditionito de sodio puede provocar la precipitación de la plata. Por el contrario, si hay una deficiencia de ditionito de sodio, es posible que el proceso de recubrimiento no se produzca correctamente o no se produzca en absoluto, especialmente porque la unidad de recubrimiento está diseñada con una baja densidad de corriente.
Configuración de la recuperación electrolítica de plata :
Tasas de recuperación y eficiencia de la plata
Al aplicar la ley de Faraday, estos cálculos proporcionan una forma de estimar la recuperación potencial de plata y la eficiencia en la desilverización electrolítica.
Masa de la sustancia = (Corriente × Tiempo × Masa equivalente) / (Constante de Faraday)
Ejemplo de cálculo Recuperación potencial: 100 A *3600 s *107,87 / 96485 = 100 A*4,02 = 402 g Ag por amperio hora
- Recuperación potencial (gramos de Ag por amperio hora) = corriente x 4,02
- Recuperación teórica %= (Recuperación potencial / Ag entrante) x 100
- Recuperación real % = (Ag saliente / Ag entrante) x 100
- Eficiencia % = (Recuperación real / Recuperación teórica) x 100