31 Jul 2025
Odzyskiwanie srebra

Srebro i oryginalny papier fotograficzny
Srebro jest niezbędnym składnikiem zapewniającym wysoką jakość wydruków na oryginalnym papierze fotograficznym. Srebro stanowi część warstwy fotograficznej, osadzonej w żelatynie. Po naświetleniu srebra (kryształów halogenku srebra) w papierze fotograficznym powstaje utajony obraz za pomocą systemu naświetlania RGB. Następnie papier fotograficzny poddaje się procesowi wywoływania RA4 z użyciem wywoływacza i utrwalacza, aby uzyskać obraz na papierze. Podczas tego procesu w trzech różnych warstwach powstają barwniki cyjan, magenta i żółty.
Jak odzyskać srebro z papieru?
Podczas procesu wywoływania RA4 około 99% srebra obecnego na zdjęciu zostaje usunięte. Ale gdzie ono trafia?
Większość tego srebra, około 96%, trafia do roztworu wybielacza-utrwalacza, gdzie łączy się z jonami tiosiarczanowymi, tworząc kompleksy. Srebro to może być odzyskiwane na miejscu przez większość dużych laboratoriów fotograficznych za pomocą elektrolitycznego usuwania srebra. Niektóre laboratoria fotograficzne mogą zdecydować się na zebranie odpadów chemicznych, które zostaną przekazane firmie zajmującej się gospodarką odpadami.
Pozostałe 3% srebra z procesu wywoływania RA4 trafia do wody popłuczkowej. Aby zapobiec utracie tego srebra wraz z wodą odpływową, niektóre laboratoria fotograficzne stosują system odsalania jonowego. System ten wykorzystuje żywice jonowymienne, które selektywnie wychwytują jony srebra z wody popłuczkowej, umożliwiając ich odzyskanie i ponowne wykorzystanie. Ten wewnętrzny proces odzyskiwania srebra zapewnia, że srebro jest odpowiednio zarządzane, zamiast być przetwarzane przez regionalną oczyszczalnię ścieków.
Jak dotąd jest to najłatwiejsza część procesu odzyskiwania srebra. Teraz przejdźmy do części technicznej:
Elektrolityczne odzyskiwanie srebra z utleniacza na bazie tiosiarczanu
Srebro występuje w roztworze wybielacza w postaci kompleksów z jonami tiosiarczanowymi, które mogą ulegać dysocjacji w stanie równowagi, uwalniając jony srebra i jony tiosiarczanowe.
Na katodzie, która jest elektrodą ujemną, jony srebra ulegają redukcji poprzez przyłączenie elektronów, tworząc srebro stałe. Reakcję tę można zapisać jako: Ag + + e –> Ag.
Na anodzie, która jest elektrodą dodatnią, może zachodzić kilka reakcji.
Ważnymi reakcjami na anodzie są utlenianie tiosiarczanu i siarczynu. Dodatkowo na katodzie zachodzi redukcja żelaza.
Reakcje te łącznie przyczyniają się do zmniejszenia stężenia tiosiarczanu, siarczynu i pH w roztworze wybielająco-utrwalającym. Skuteczność roztworu wybielająco-utrwalającego można przywrócić poprzez napowietrzanie, które przekształca nieaktywne jony Fe2+ w aktywne jony Fe3+.
Aby zapewnić skuteczne usuwanie srebra, konieczne jest wystarczające mieszanie, aby zapobiec tworzeniu się siarczku srebra na katodzie.
Żelatyna jest pożądana tylko do około 2% masy srebra, ponieważ jej nadmiar może również prowadzić do siarczkowania.
Należy pamiętać, że odbarwianie w roztworach wybielająco-utrwalających jest trudniejsze w porównaniu z odzyskiwaniem utrwalacza, ze względu na udział reakcji żelaza III i żelaza II. Aby przeciwdziałać ponownemu utlenianiu żelaza, zazwyczaj stosuje się system wysokoprądowy.
Mniej popularnym alternatywnym systemem ciągłego odbarwiania jest PSR (Ilford) Electrogen. System ten wykorzystuje kontrolowaną redukcję żelaza III do żelaza II za pomocą ditionitu sodu. Aby zapewnić precyzyjne dozowanie, stosuje się sondę i jednostkę dozującą, które zapobiegają dodaniu nadmiernej ilości odczynnika. Dodanie nadmiernej ilości ditionitu sodu może spowodować wytrącenie się srebra. Z drugiej strony, jeśli występuje niedobór ditionitu sodu, proces powlekania może nie przebiegać prawidłowo lub w ogóle nie nastąpić, zwłaszcza że jednostka powlekająca została zaprojektowana z niską gęstością prądu.
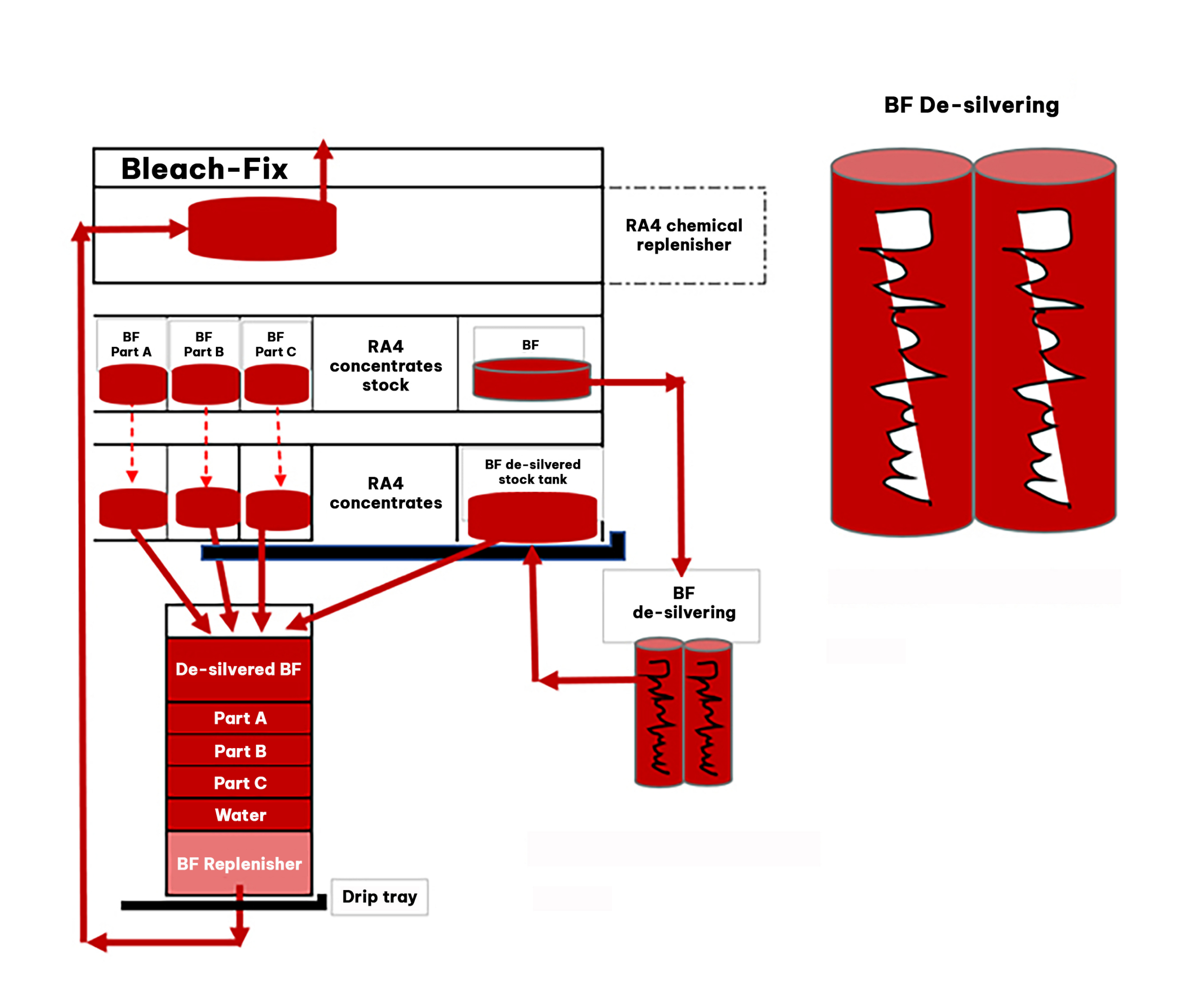
Konfiguracja elektrolitycznego odzyskiwania srebra :
Współczynniki odzysku srebra i wydajność
Stosując prawo Faradaya, obliczenia te pozwalają oszacować potencjalny odzysk srebra i wydajność w procesie elektrolitycznego usuwania srebra.
Masa substancji = (prąd × czas × masa równoważna) / (stała Faradaya)
Przykładowe obliczenia Potencjalny odzysk: 100 A *3600 s *107,87 / 96485 = 100 A*4,02 = 402 g Ag na amperogodzinę
- Potencjalny odzysk (gramy Ag na amperogodzinę) = prąd x 4,02
- Teoretyczny odzysk %= (potencjalny odzysk / Ag_in) x 100
- Rzeczywisty odzysk % = (Ag_out / Ag_in) x 100
- Wydajność % = (rzeczywisty odzysk / teoretyczny odzysk) x 100